蛋白沉积性罕见病的诊断标志物与检测策略
本文系统介绍蛋白沉积性罕见病(即淀粉样变性)在临床诊断与检测中的关键标志物与实践策略,覆盖血液与尿液生物标志物、影像学与组织学检查、基因检测、心血管与神经学专科评估,以及药理学、免疫治疗与移植相关的检测要求,并讨论长期监测、多学科管理、临床试验参与与本地服务的可及性与筛查路径,面向需要系统检测与分型指导的读者。
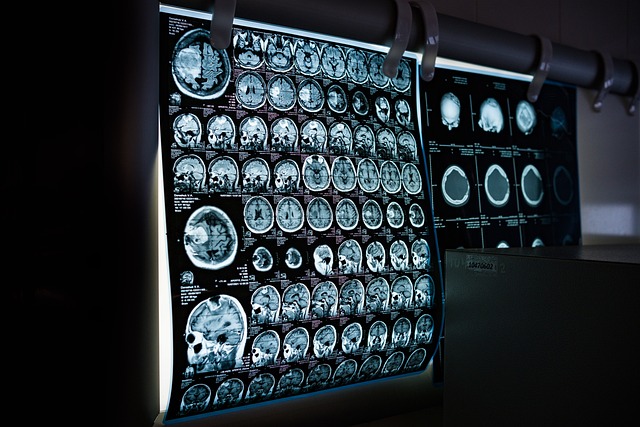
蛋白沉积性罕见病(通常称为淀粉样变性)是一组由异常蛋白折叠并在组织或器官中沉积所致的疾病,常累及心脏、神经系统、肾脏与消化道等多个系统。不同类型(如免疫球蛋白相关的AL型或转甲状腺素蛋白相关的ATTR型)在致病机制、进展速度和可用治疗上存在显著差异,因此早期识别并进行精确分型对于临床决策、预后评估和临床试验入组都十分重要。有效的检测策略通常将血清与尿液生物标志物、影像学检查、必要时的组织活检与分子遗传学检测相结合,同时强调在本地医疗服务体系中建立可及的筛查和转诊流程,以便患者迅速进入专科评估与管理通道。
本文章仅供信息参考,不构成医疗建议。请咨询合格的医疗专业人员以获得个体化诊疗方案。
biomarkers与筛查策略
生物标志物在早期筛查和疗效监测中发挥核心作用。用于筛查的常规检测包括血清免疫固定电泳、尿液免疫固定电泳、游离轻链(FLC)定量及FLC比率,以提示是否存在浆细胞克隆相关的AL型。用于心脏受累评估的标志物如高敏肌钙蛋白和NT-proBNP可反映心肌损伤和心功能负荷。对组织样本的质谱分析或特异性免疫组化可帮助鉴定沉积蛋白的具体类型,从而指导分型和后续治疗决策。
如何进行早期diagnosis与临床筛查
早期诊断依赖于临床对非特异性症状的高度警觉,如不明原因的充血性心力衰竭伴保留射血分数、周围神经病变、自主神经功能异常、蛋白尿或进行性体重下降。合理的临床路径通常先进行基础实验室与生物标志物筛查,随后依据结果进行影像学评估(心脏超声、心脏MRI或放射性核素显像)和必要的活检检查(皮肤、肾脏或心脏活检)以确认沉积与分型。建立在本地服务(local services)基础上的快速转诊机制有助于减少诊断延迟。
genetics在病因与分型中的作用
遗传学在某些亚型(尤其是家族性ATTR)中具有决定性意义。基因检测可识别如TTR等基因的致病性变异,影响治疗选择、随访策略以及家族成员的筛查决策。检测前后的遗传咨询非常重要,以解释结果的临床意义及家族风险。对于年轻发病或疑难病例,扩展基因面板可用于发现罕见致病变异并为个体化治疗或临床试验入组提供依据。
cardiology与neurology的专科检测
心血管和神经系统为常见受累位点,需专科评估以确定受累程度。心脏评估包括心电图、心脏超声(评估室壁厚度与舒张功能)、心脏MRI以及99mTc-PYP/DPD等核医学检查(对ATTR具有提示价值),并结合NT-proBNP与肌钙蛋白监测病情变化。神经学评估则包括临床功能检查、神经传导速度测试以及必要时的皮肤或神经活检用于小纤维或轴突性损害的评估。专科间的讨论有助于将影像学、生化与组织学结果整合形成全面诊疗方案。
pharmacology、immunotherapy与transplant的治疗相关检测
治疗方案由病理分型决定:AL型侧重于针对浆细胞克隆的化疗或免疫治疗,需骨髓活检、流式细胞术及免疫球蛋白谱检测以指导疗效评估;ATTR型则有多种靶向药物(如TTR稳定剂、RNA干扰或反义寡核苷酸)可用于抑制致病蛋白生成或促进降解,治疗前后均需定期检测生物标志物和器官功能。免疫治疗在部分研究中用于清除沉积蛋白或调控免疫反应,但需基于分型和临床试验证据。对于器官功能严重受损者,器官移植(心或肝)仍可能是合理选择,移植前需全面多器官评估与风险评估。
monitoring、symptommanagement与multidisciplinary的长期随访
长期监测应结合生物标志物(FLC、NT-proBNP等)、影像学和功能性评估,以评估治疗反应与疾病进展。症状管理侧重心衰对症治疗、疼痛与神经病变控制、肾功能支持、康复与营养干预。多学科团队(心内科、血液科、神经科、肾内科、遗传咨询、康复与护理)在患者护理、临床试验对接和提高医疗可及性(accessibility)方面发挥关键作用。建议在本地服务与专科中心之间建立有效转诊和信息共享机制,以便患者获得及时评估和适合的临床研究机会(clinicaltrials)。
结论:蛋白沉积性罕见病的诊断与管理依赖于多模态检测与精确分型,从血液与尿液生物标志物、影像学与组织学到遗传学检测的综合应用。系统化筛查路径、多学科协作与个体化长期监测有助于提高诊断效率与患者护理质量,随着药理学与免疫治疗研究进展,精准分型与临床试验参与将继续影响治疗选择与预后评估。




